Innhold
- Hovedforskjell
- Sammenligningstabell
- Hva er spesifikk varme?
- Hva er varmekapasitet?
- Spesifikk varme vs. varmekapasitet
Hovedforskjell
Varme er en av formene for energier, når to gjenstander samvirker at overføringen av denne energien fra en kropp til en annen er mye sannsynlig. Varmeenergi er direkte proporsjonal med temperaturen, betyr at økningen i temperaturen automatisk vil trekke til økningen i varmeenergi i kroppen og omvendt. Begge disse begrepene, spesifikk varme og varmekapasitet er mye brukt i termodynamikk, da begge refererer til energien som kreves for å øke temperaturen til et objekt. Spesifikk varme og varmekapasitet er ganske lik hverandre med bare en forskjell på tilleggsvariabel i den spesifikke varmen. Selv om mange bruker disse begrepene om hverandre, ettersom konseptet deres samlet beskrives som "spesifikk varmekapasitet". For å få forskjellen mellom begge disse begrepene, må man vite om tilleggsvariabelen i den spesifikke varmen. Varmekapasitet er den mengden varme som kreves for å øke temperaturen til et stoff til 1 grad Celsius (°C) eller 1 Kelvin, mens spesifikk varme er den mengden varme som er nødvendig for å øke temperaturen på stoffet som har masse 1 kg eller 1 g med 1 grad Celsius (°C) eller 1 Kelvin.
Sammenligningstabell
| Spesifikk varme | Varmekapasitet | |
| Definisjon | Spesifikk varme er mengden varme som kreves for å øke temperaturen på stoffet som har masse 1 kg eller 1 g med 1 grad Celsius (° C) eller 1 Kelvin. | Varmekapasitet er mengden varme som kreves for å øke temperaturen til et stoff til 1 grad Celsius (° C) eller 1 Kelvin. |
| Masse | Spesifikk varme er direkte proporsjonal med gjenstandens eller stoffets masse. | Varmekapasitet avhenger ikke av massen. |
| SI-enheter | J kg-1 K-1 | J / K |
Hva er spesifikk varme?
Den spesifikke varmen ligner veldig på varmekapasiteten, ettersom begge deler innebærer å bringe en enhet temperaturøkning i en kropp, selv om den blir annerledes med sistnevnte, fordi den har en ekstra variabel, 'Mass' som må holdes lagt merke til mens du legger merke til at en enhet med temperaturøkning. Den spesifikke varmen til vann er 4.186 Jg-1oC-1, med enkle ord kan vi si at for å øke 1 oC i 1 gram vann trenger vi 4.186 Joule varmeenergi. Forholdet mellom varme og temperatur kan uttrykkes som:
Q = cm ∆T,
hvor,
Q er Heat Added
C er spesifikk varme
∆T er temperaturendring
Forholdet forblir ikke gyldig når en faseendring oppstår, betyr konvertering av vann til gassformig tilstand (kokepunkt) eller når isen konverterer til flytende tilstand (smeltepunkt. Det er fordi varmen fjernet eller tilført under faseendringen gjør det ikke føre til endring i temperaturen. Når det handler om teoretisk arbeid eller laboratoriearbeid, brukes spesifikk varme i stedet for varmekapasitet, da den også måler stoffets eller gjenstandens masse.
Hva er varmekapasitet?
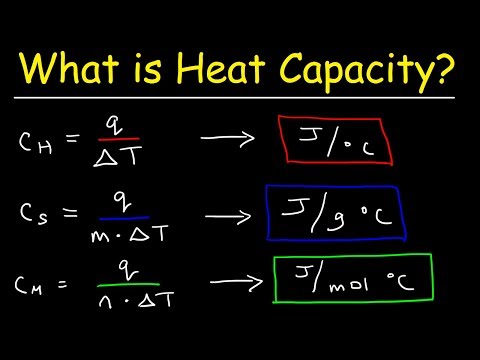
Varmekapasitet er mengden varme som kreves for å øke temperaturen til et stoff til 1 grad Celsius (° C) eller 1 Kelvin. Varmen som trekkes inn eller temperaturøkningen har ikke noe med stoffets masse å gjøre. Varmeenergi er direkte proporsjonal med temperaturen, betyr at økningen i temperaturen automatisk vil trekke til økningen i varmeenergi i kroppen og omvendt. Varmekapasitet kan defineres ved hjelp av denne ligningen:
C = ∆Q / ∆T,
Hvor,
Δ Q er mengden varme som er tilsatt
C er den spesifikke VARME
Δ T er temperaturendringen
Spesifikk varme vs. varmekapasitet
- Varmekapasitet er den mengden varme som kreves for å øke temperaturen til et stoff til 1 grad Celsius (° C) eller 1 Kelvin, mens spesifikk varme er mengden varme som kreves for å øke temperaturen på stoffet som har masse 1 kg eller 1 g med 1 grad Celsius (° C) eller 1 Kelvin.
- Spesifikk varme er direkte proporsjonal med gjenstandens eller stoffets masse, mens varmekapasiteten ikke avhenger av massen.
- J / K er SI-enheten for varmekapasitet, mens J kg-1 K-1 er SI-enheten for spesifikk varme.
