Innhold
- Hovedforskjell
- Fordampning kontra kondens
- Sammenligningstabell
- Hva er fordampning?
- Eksempel
- Hva er kondens?
- Eksempel
- Viktige forskjeller
- Konklusjon
Hovedforskjell
Hovedforskjellen mellom fordampning eller kondensering er at fordampning er prosessen med å endre flytende tilstand til en gassform, mens kondensering er prosessen med å endre gassform til flytende tilstand.
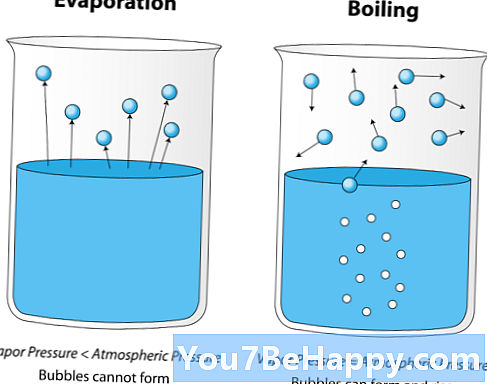
Fordampning kontra kondens
Fordampning er prosessen der et stoff endrer seg fra sin flytende fase til gassfase, mens kondensering er prosessen der et stoff endrer seg fra sin gassfase til flytende fase. Fordampning skjer ved en hvilken som helst temperatur rett under kokepunktet, men kondensering skjer ved konstant temperatur. Fordampning skjer når energinivået til et stoff øker og får molekylene til å bevege seg raskere og unnslippe fra overflatespenning til omgivelsene, på den annen side oppstår kondensasjon når temperaturen redusert i volum av luft mettet til stoffmolekyler forårsaker kondens når molekylene mister energi og begynn å kombinere til de blir dråper løsningen. Fordampning skjer når trykket er lavt, og temperaturen er høy, tvert imot, kondensering skjer når trykket er høyt, men senker temperaturen. Ved fordampning oppvarmes en væske tilstrekkelig, og tiltrekningskreftene mellom molekyler forhindrer dem ikke i å bevege seg hver for seg, deretter fordampes væsken til gass, på baksiden, i kondens, gass-avkjølt tilstrekkelig og tiltrekningskreftene mellom molekyler hindre dem i å bevege seg separat, så kondenserer gassen til væske eller fast stoff. Fordampning kan skje hele tiden, på alle overflater og alle steder, mens kondens bare skjer ved karbonpartikler, hygroskopiske kjerne-pollenkorn og på salter, etc.
Sammenligningstabell
| fordampning | Kondensasjon |
| Fordampning er en prosess for å endre væskefasen til damper / gasser. | Kondensering er prosessen med å endre damper / gasser til væske eller dråper vann. |
| Faseendring | |
| Bytt fra væske til damp. | Bytt fra damp til væske. |
| Påvirke på omgivelsene | |
| Den absorberer energi fra omgivelsene. | Slipper energi til omgivelsene. |
| Temperaturpunkt | |
| Temperaturen når som helst rett under kokepunktet. | Temperaturen forblir konstant. |
| Forhold | |
| Temperaturen er høy; trykket er lavt. | Trykket er høyt; temperaturen er lav. |
| Hendelse | |
| Hele tiden, på alle overflater og alle steder. | Bare foregår ved karbonpartikler og på salter etc. |
| Force of Attraction | |
| Ikke hindre dem i å bevege seg separat. | Hindre dem fra å bevege seg separat. |
| Kinetiske energier | |
| Den har et stort utvalg av kinetiske energier. | Den har et lite utvalg av kinetiske energier. |
Hva er fordampning?
Fordampning er prosessen der et stoff endrer seg fra sin flytende fase til sin gassfase. Fordampning skjer når trykket er lavt, og temperaturen er høy. Ved fordampning oppvarmes en væske tilstrekkelig, og tiltrekningskreftene mellom molekyler forhindrer dem ikke i å bevege seg hver for seg; så fordamper væsken til gassform. Fordampning skjer ved en hvilken som helst temperatur rett under kokepunktet. Fordampning skjer når energinivået til et stoff øker og får molekylene til å bevege seg raskere og flykte fra overflatespenning til omgivelsene. Ved fordamping tar de opp energi fra omgivelsene. Den kinetiske energien til flytende molekyler er høy, og noen har nok energi til å overvinne attraktive krefter som holder dem bundet, og ved å bruke den energien blir molekyler begeistret, og på et eller annet nivå når de maksimalt metningsnivå som får dem til å konvertere til gassform . Fordampning spiller en viktig rolle i vannsyklusen der molekyler blir ført opp av vinden og kondenserer til slutt i form av skyer som forårsaker regn. Fordampning skjer i lave høyder hele tiden, på alle overflater og alle steder.
Eksempel
Svetten på den ytre overflaten av et kaldt glass fordamper når glasset blir varmt.
Hva er kondens?
Kondensering er metoden der et stoff endres fra sin gassfase til flytende fase eller til små dråper vann. Kondensering oppstår når temperaturen redusert i volumet av luft mettet til stoffmolekyler forårsaker kondensering ettersom molekylene mister energien og begynner å kombinere til de blir dråper av løsningen. Kondensering skjer når trykket er høyt, men temperaturen sank. Eksotermiske reaksjoner oppstår ved kondens og energi frigjort til omgivelsene, noe som forårsaker en økning i temperaturen. Kondensasjonen er også faseendringen uavhengig av temperaturen. Kondensering skjer hovedsakelig i større høyder og karbonpartikler, hygroskopiske kjerne-pollenkorn og på salter, etc.Kondensasjon spiller også en rolle i vannsyklusen der molekyler blir ført opp av vinden; så kondenserer de til slutt i form av skyer som forårsaker regn.
Eksempel
Vanndamp kondenserer og danner svette på utsiden av glasset eller boksen.
Viktige forskjeller
- Fordampning er prosessen med å endre flytende tilstand til en gassform, mens kondensering er prosessen med å endre gassform til flytende tilstand.
- Fordampning skjer ved en hvilken som helst temperatur rett under kokepunktet, men kondensering skjer ved konstant temperatur.
- Fordampning skjer når energinivået til et stoff øker og får molekylene til å bevege seg raskere og unnslippe fra overflatespenning til omgivelsene, på den annen side oppstår kondensasjon når temperaturen redusert i volum av luft mettet til stoffmolekyler forårsaker kondens når molekylene mister energi og begynn å kombinere til de blir dråper løsningen.
- Fordampning skjer når trykket er lavt, og temperaturen er høy, tvert imot, kondensering skjer når trykket er høyt, men senker temperaturen.
- Fordamping absorberer energi fra omgivelsene, mens kondens frigjør energi til omgivelsene.
- Fordampning kan skje hele tiden, på alle overflater og alle steder, mens kondens bare skjer ved karbonpartikler, hygroskopiske kjerne-pollenkorn og på salter, etc.
Konklusjon
Diskusjonen ovenfor konkluderer med at fordampning er prosessen med å endre flytende tilstand til en gassform, mens kondensering er prosessen med å endre gassform til flytende tilstand.